【www.guakaob.com--质量工程师】
绝密★启用前
2016年江苏省普通高中学业水平测试(必修科目)试卷
化 学
本卷可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32
Cl:35 .5 Fe:56 I:127 Ba:137.
一、单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分)。 1.在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于
A.提出了元素周期律 B.开发了合成氨的生产工艺 C.揭示了燃烧的本质 D.提取了治疟药物青蒿素 2.近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配
以相应的文字形成的(如右图所示)。苯()属于 A.氧化物 B.硫化物 C.无机物 D.有机物 3.下列变化属于物理变化的是
A.煤的燃烧 B.碘的升华 C.铜的锈蚀 D.铝的冶炼 4.研究化学反应常用18 8O作为示踪原子,该原子的质子数是 A.18 B.8 C.10 D.16 5.下列化学用语表示正确的是
A.氯气的电子式: B.乙烯的结构简式CH2CH2
C.钠原子的结构示意图:
+
-
D.硫酸亚铁的电离方程式FeSO
4Fe2+SO42 6.下列气体可用向上排空气法收集的是
A.NH3 B.H2 C.Cl2 D.CH4
7.实验室用大理石和盐酸制备CO2。下列措施可使反应速率加快的是 A.降低反应温度 B.延长反应时间 C.粉碎大理石 D.加水稀释盐酸 8.下列物质含有离子键的是
A.HCl B.NaCl C.N2 D.
NO
9.下列常见物质的俗名与化学式对应正确的是 A.烧碱--NaOH B.小苏打——Na2SO4 C.熟石灰——CaCl2 D.明矾——Al2(SO4)3
--2+
10.在含有大量的Ba、OH、Cl的溶液中,还可能大量共存的离子是
--++
A.CO32 B.NO3 C.H D.Fe3
11.实验室可用右图所示的装置制备少量氧气,下列说法正确的是 A.实验前需检查装置的气密性
B.当水槽中导管口一有气泡逸出时,就立即收集氧气 C.实验结束时先撤走酒精灯,再从水槽中取出导管 D.常温下将木条伸入盛有氧气的集气瓶中,木条自燃 12.下列属于吸热反应的是
A.镁的燃烧反应 B.盐酸与氢氧化钠的反应 C.水的分解反应 D.铝与氧化铁的铝热反应 13.工业上可用金属钠和氯化钾反应制备金属钾,期化学方程式为:Na+KClNaCl+K↑。该反应属于
A.置换反应 B.复分解反应 C.分解反应 D.化合反应 14.下列有关甲烷的说法正确的是
A.易溶于水 B.是天然气的主要成分 C.与氯气发生加成反应 D.与乙烷互为同分异构体 15.工业上制备硝酸的一个重要反应为:4NH3+5O
2
4NO+6H2O。下列有关该反应的说法正确
的是
A.O2是还原剂 B.NH3是氧化剂 C.O2失去电子 D.NH3发生氧化反应 16.用NA表示阿伏伽德罗常数的值。下列判断正确的是 A.1mol H2含有的分子数目为NA
+
B.24g Mg变为Mg2时失去的电子数目为NA
--
C. 1L 1mol·L1CaCl2溶液中含有的Cl离子数目为NA D.常温常压下,11.2LO2中含有的原子数目为NA 17.下列反应的离子方程式书写正确的是
+【2016年江苏省普通高中学业水平测试(必修科目)热身卷化学】
A.FeCl3溶液与Cu反应:Fe3+ Cu = Fe2+ + Cu2+
+—
B.AgNO3溶液与NaCl反应:Ag + Cl = AgCl↓
—
C.Cu(OH)2与CH3COOH反应:OH+ H+=H2O
-+
D.CaCO3与HNO3反应:CO32+2H = H2O + CO2↑ 18.下列实验方法能达到实验目的的是 A.用分液漏斗从食醋中分离出乙酸 B.用焰色反应鉴别Na2SO4和Na2CO3
C.用NaOH溶液除去Cl2中含有的少量HCl
+
D.用KSCN溶液检验FeCl3溶液 中是否含有Fe3 19.右图是土豆电池的示意图。土豆电池工作时,
下列有关说法正确的是 A.Fe用作正极 B.Cu片质量减少
C.电子由Fe并经导线流向Cu片 D.实现了电能向化学能的转化
20.在化学魔术中,一张白纸在用碘溶液喷洒后会呈现出蓝色字迹,其奥秘在于这张白纸曾经一种“隐秘墨水”书写过。这种“隐秘墨水”为
A.食盐水 B.白醋 C.淀粉溶液 D.蔗糖溶液 21.下列有关乙醇性质的化学方程式正确的是 A.与金属钠反应: 2CH3CH2OH+2Na2CH3CH2ONa+H2↑
Cu
B.与氧气的燃烧反应:2CH3CH2OH+O2―△―→2CH3CHO+2H2O
点燃 C.与氧气的催化氧化:CH3CH2OH+3O22CO2+3H2O
D.与乙酸的酯化反应:CH3COOH+CH3CH2OH
CH3COOCH2CH
3
22.X、Y、Z、W是原子序数依次增大的短周期主族元素。Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4。下列说法正确的是 A.原子半径:r(W)>r(Z)>r(Y)>r(X) B.Y的简单气态氢化物的热稳定性比Z的强
C.由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 D.由X、Y、Z三种元素组成的化合物可以是酸、碱或盐
-
23.将5.10g镁铝合金加入120mL4.0mol·L1的盐酸中,待合金完全溶解后,得到溶液X。下列说法一定正确的是
A.合金完全溶解后产生的H2的物质的量为0.24mol B.合金中的镁与铝的物质的量之比小于1
-
C.若向溶液X中加入270mL2.0mol·L1NaOH溶液,充分反应,所得沉淀为Mg(OH)2
D.若向溶液X中加入足量的氨水,充分反应,所得沉淀经过过滤、洗涤后充分灼烧,则残留固体质
量大于8.50g.
二、非选择题(本部分3题,共31分) 24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基
础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。 A.《化学与生活》
(1)(3分)2015年11月首架C919打飞机总装下线,标志着我
国跻身飞机研制先进国家行列。
①机身蒙皮使用的是第三代铝锂合金材料。下列不属于铝锂 合金性质的是 ▲ (填字母)。
a.密度大 b.硬度大 c.抗腐蚀
②飞机轮胎属于橡胶制品。下列材料可用来合成橡胶的是
▲ (填字母)。
a.石英砂 b.石灰石 c.异戊二烯
③机体先进复合材料的使用率达12%。下列属于复合材料的是。 a.钛合金 b.玻璃钢 c.普通陶瓷
(2)(5分)秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰
富的铁、锌、钙等元素,其中:
①属于人体所需微量元素的是 ▲ 。 ②属于水溶性维生素的是
。
③蛋白质在人体内最终的水解产物是 ▲ 。 (3)(7分化学能帮助我们更好地认识生活、改善生活。
①家用铁锅未洗净晾干,放置一段时间后出现红褐色锈斑,其主要的原因是铁发生了 ②乘车禁止携带物品的部分标识如右图所示。在
浓硝酸、食盐、汽油、石膏四种物品中,不能 携带上车的是 ▲ 。
③过氧乙酸()易分解为乙酸和氧气,
其稀溶常用于餐具、器械的消毒。协会粗过氧乙酸分解的化学方程式 ▲ 。某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式 ▲ 。 25.(6分)有关物质的转化关系如下图所示(部分生成物与反应条件已略去)。A是常见的非金属固体单
质,F是紫红色的金属单质,B、C是常见的强酸,D、G、I是常见的气体,D与I
的组成元素相同,
且D的相对分子质量比I的大16。E是最常见的无色液体。
请回答下列问题:
(1)E的电子式为 (2)H的化学式为。
(3)写出反应①的化学方程式:。
(4)写出反应③的离子方程式:。 26.(10分)亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下: NaOH溶液 SO2 Na2SO3产品 Na2CO3【2016年江苏省普通高中学业水平测试(必修科目)热身卷化学】
查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中, 溶液中有关组分的质量分数变化如右图是所示。
(1)右图中的线2表示的组分为 ▲ (填化学式) (2)实验时,“反应II”中加入NaOH溶液的目的
是 ▲ (用化学方程式表示)
(3)国家标准规定产品中Na2SO3的质量分数≥97.0%
为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了两种方法进行测定。 ①方法I:称取2.570g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,在加
入过量的BaCl2溶液,所得沉淀经过过滤、洗涤、干燥后称量,质量为4.660g,通过计算确定产品中Na2SO3的质量分数(写出计算过程)
②方法II:称取1.326g产品,配成100mL溶液,取25.00mL该溶液,滴加0.1250mol/L I2溶液,恰好使Na2SO3完全氧化生成Na2SO4时,消耗I2溶液20.00mL。通过计算确定产品中Na2SO3的质量分数(写出计算过程)
③判断Na2SO3产品的等级,并说明理由。
2016年江苏省普通高中学业水平测试(必修科目)试卷
化学参考答案
一、单项选择题(共69分)
24.(15分) A.《化学与生活》 (1)(3分)
①a ②c ③b
(2)(5分)
①铁、锌
②维生素C 纤维素 (3)(7分) ①电化学 ② 浓硝酸、汽油
③2CH3COOH→2CH3COOH+O2↑;
2AlbMgc(OH)mCO3 +(6b+4c) HCl=2b AlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑
25.(6分) (1)
(2)CuSO4
(3)S+6HNO3 (浓) (4)H2O+NO2+SO226.(10分)
H2SO4+6NO2↑+H2O 2H+SO42+NO
+
-
(1)NaHCO3
(2)NaHSO3+NaOH=Na2SO3+H2O (3)①98.05%
②95.02%
③产品为一等品。产品中含有的硫酸钠和碳酸钠,在方案I的测定中,硫酸钠和碳酸钠杂质使得
测定值偏高。而方案II是直接测定亚硫酸钠,更可信。
绝密★启用前
2015年江苏省普通高中学业水平测试(必修科目)试卷
化 学
本卷可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Al:27 S:32
Cl:35.5 K:39 Fe:56
一、单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,
共69分)。
1.手机芯片是一种在半导体材料上集合多种电子元器件的电路模块。下列可用作半导体材料的是
A.铝 B.硅 C.碳 D.铁 2.下列物质属于酸的是
A.KCl B.O2 C.NaOH D.HNO3 3.下列过程只涉及物理变化的是
A.伐薪烧炭 B.酿酒成醋 C.滴水成冰 D.百炼成钢 4.工业焊接钢管时常用137 ,这里的“137”是指该原子的 55Cs进行“无损探伤”
A.质子数 B.中子数 C.电子数 D.质量数 5.实验室由海水获得淡水的实验装置是
A B C
D
6.通入水中所得溶液呈碱性的气体是
A.NH3 B.NO2 C.SO2 D.HCl 7.下列物质属于共价化合物的是
A.CaO B.CO2 C.K2O D.NaCl 8.漂白粉的有效成分是
A.Ca(ClO)2 B.CaCl2 C.Ca(OH)2 D.CaCO3 9.反应2SO2+O22SO3在密闭容器中进行。下列关于该反应的说法错误的是 ..
A.升高温度能加快反应速率 B.使用恰当的催化剂能加快反应速率 C.增大O2的浓度能加快反应速率 D.SO2与O2能100%转化为SO3 10.在含有大量的Na+、OH、NO3,该溶液中还可能大量存在的离子是
—
A.NH4+ B. H+ C. SO42 D.Mg2+
—
—
11.下列化学用语表示正确的是
A.乙酸的结构简式:C2H4O2 B.Cl的结构示意图: C.H2O的电子式: D.XX的电离方程式:XXX 12.下列过程吸收热量的是
A.汽油燃烧 B.氨气液化 C.碳酸钙分解 D.浓硫酸稀释 13.实验室制备硅酸的反应为Na2SiO3+2HCl=2NaCl+H2SiO3↓,该反应属于
A.化合反应 B.分解反应 C.置换反应 D.复分解反应 14.下列有机反应属于加成反应的是
光照____ A.CH3CH3 + Cl2 → CH3CH2Cl + HCl B.CH2==CH2+HBr→CH3CH2Br
Cu
C.2CH3CH2OH+O2―△―→2CH3CHO+2H2O
CH3COOCH2CH3+H2O 15.下列有关物质用途的说法正确的是
A.明矾可用作净水剂 B.甲醛可用作食品防腐剂 C.氢氧化钠可用来治疗胃酸过多 D.铝制容器可长期存放酸性食物 16.用NA表示阿伏伽德罗常数的值。下列判断正确的是 A.28g N2含有的氮原子数目为NA
B.常温常压下,22.4L Cl2含有的分子数目为NA C.1molNa变为Na+时失去的电子数目为NA D.1L 1mol·L—1K2CO3溶液中含有的钾离子数目为NA
17.中国最新战机歼-31使用了高强度、耐高温的钛合金材料。工业上冶炼钛的反应如下:
高温
TiCl+
2Mg
Ti+2MgCl 。下列有关该反应的说法正确的是 D.CH3COOH+CH3CH2OH
4
—
2
A.TiCl4是还原剂 B.Mg被氧化 C.TiCl4发生氧化反应 D.Mg得到电子 18.下列关于乙烯的说法正确的是
A.是天然气的主要成分 B.能使溴的四氯化碳溶液褪色 C.不能发生燃烧反应 D.不能发生加聚反应
19.下列关于Cl2性质的说法正确的是
A.密度比空气小 B.是无色无味的气体 C.能使干燥的有色布条褪色 D.可与NaOH溶液反应 20.下列反应的离子方程式书写正确的是
A.锌粒与稀盐酸反应:Zn + 2H+ = Zn2+ + H2↑
——
B.溴化钠溶液与氯气反应:Br + Cl2 = Cl + Br2
—
C.氢氧化铜与稀硫酸反应:OH+ H+=H2O
—
D.钠与水反应:Na +2H2O = Na++ 2OH+ H2↑ 21.“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O = 2Mg (OH)2 。下列关于该电池的说法错误的是
A.镁片作为正极 B.食盐水作为电解质溶液
C.电池工作时镁片逐渐被消耗 D.电池工作时实现了化学能向电能的转化
22.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族。下列说法正确的是
A.X与Y只能形成一种化合物 B.原子半径:r(Y)<r(W)<r(Z)
C.W的简单气态氢化物的热稳定性比Y的强 D.Z的最高价氧化物对应的水化物是酸
23.实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是
A.取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一
定含有Na2CO3
B.取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,
说明原固体中一定含有Na2CO3
C.取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原
固体中一定含有NaCl
D.称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分
反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3
二、非选择题(本部分3题,共31分)
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有
机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。 A.《化学与生活》
(1)(3分)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于(填字母)。 a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是。 a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和。
a.石灰石 b.粗盐 c.纯碱 (2)(5分)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为 ▲ 、糖类和蛋白质。淀粉在人体内水解的最终产物是 ▲ 。
②维生素是人体需要的营养物质。右图为某品牌维生素
C泡腾片说明书的部分内容。该泡腾片中添加的着色 剂是 ▲ ,甜味剂是 ▲ 。泡腾片溶于 水时产生“沸腾”效果,是由于添加的酒石酸和 ▲ 反应释放出了气体。
(3)(7分)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。 ①控制燃煤产生的SO2排放,能够减少 ▲ 型酸雨的形成。燃煤排放的烟气中还含有
其他污染物,请列举一种: ▲ 。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵
(NH4HCO3),写出该反应的化学方程式 ▲ 。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是 ③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为 25.(6分)有关物质的转化关系如下图所示(部分物质与条件已略去)。A是常见的金属单质,
B是常见的强酸,E是空气中含量最多的单质,I是既能与强酸又能与强碱反应的氧化物,G是最常见的无色液体,J是一种高硬度材料(摩尔质量为41g ·mol—1)。
请回答下列问题:
(1)D的化学式为 (2)F的电子式为。
(3)写出反应①的离子方程式: (4)写出反应②的化学方程式:
26.(10分)某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42 + 16H+
—
(1)加入FeS2还原后,检验Fe3+是否反应完全的试剂为 ▲ 。 (2)所得FeCO3需充分洗涤,检验是否洗净的方法是 ▲ 。“沉淀”时,pH不
宜过高,否则制备的FeCO3中可能混有的杂质是 ▲ 。 (3)①写出“还原”时反应Ⅱ的离子方程式: ▲ 。
②“还原”前后溶液中部分离子的浓度见下表(溶液体积变化或略不计):
请计算反应Ⅰ、Ⅱ中被还原的Fe的物质的量之比(写出计算过程)。
绝密★启用前
2015年江苏省普通高中学业水平测试(必修科目)试卷
化 学
S:32 Cl:35.5 K:39 Ca:40 Cr:52 Fe:56 Zn:65 Ba:137
一、单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,
共69分)。 1.(2015·1)手机芯片是一种在半导体材料上集合多种电子元器件的电路模块。下列可用作半导体材料的是 ( ) A.铝 B.硅. C.碳 D.铁 2.(2015·2)下列物质属于酸的是 A.KCl B.O2 C.NaOH 3.(2015·3)下列过程只涉及物理变化的是 A
.伐薪烧炭
B.酿酒成醋
C.滴水成冰【2016年江苏省普通高中学业水平测试(必修科目)热身卷化学】
.
(
D.HNO3. ( D.百炼成钢
) )
4.(2015·4)工业焊接钢管时常用137,这里的“137”是指该原子的( ) 37Cs进行“无损探伤” A
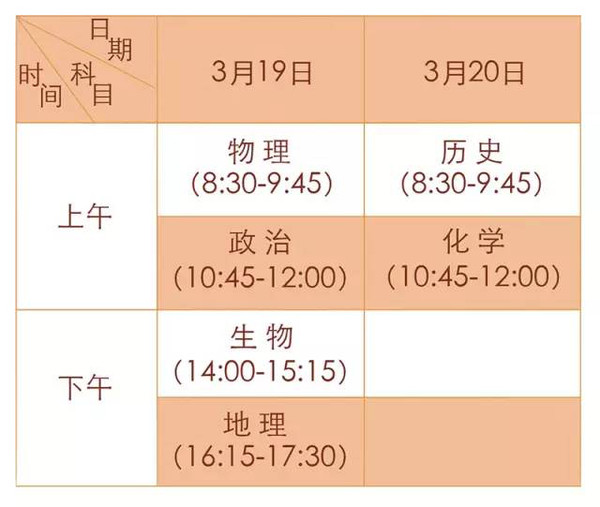
.质子数 B.中子数 C.电子数 5.(2015·5)实验室由海水获得淡水的实验装置是
D.质量数. (
)
A.
B.
C.
D.
1
2016年江苏省普通高中学业水平测试
(必修科目)说明
化 学
一、命题指导思想
化学(必修科目)学业水平测试的命题,以《普通高中化学课程标准(实验)》和《江苏省普通高中化学课程标准教学要求(修订稿)》为依据,以化学必修科目所要求的基础知识、基本技能、基本思想和基本方法为主要考查内容,注重考查学生的基本化学素养,同时兼顾考查学生分析、解决问题的能力和初步的科学探究能力,引导学生关注与化学有关的科学技术、社会经济和生态环境的协调发展,促进学生在知识与技能、过程与方法、情感态度与价值观等方面的全面发展。
二、测试内容和要求
(一)测试范围
必修模块《化学1》和《化学2》,选修模块《化学与生活》、《有机化学基础》二者选一,以及相关的初中化学教学内容(其内容本说明中不再列出)。
(二)测试能力要求的表述
参照《普通高中化学课程标准(实验)》及《江苏省普通高中化学课程标准教学要求(修订稿)》对认知性、技能性、体验性三类学习目标的分类方法、水平层次划分和各层次中的行为动词,相应地将认知性测试要求由低到高分为A、B、C、D四个水平层次,技能性测试要求由低到高分为a、b、c三个水平层次,体验性测试要求由低到高分为Ⅰ、Ⅱ、Ⅲ三个水平层次。高水平层次的测试要求包含低水平层次的测试要求。
1.认知性测试要求的水平层次
A.知道、说出、识别、描述、举例、列举
B.了解、认识、能表示、辨认、区分、比较
C.理解、解释、说明、判断、预期、分类、归纳、概述
D.应用、设计、评价、优选、使用、解决、检验、证明
2.技能性测试要求的水平层次
a.初步学习、模仿
b.初步学会、独立操作、完成、测量
c.学会、掌握、迁移、灵活运用
3.体验性测试要求的水平层次
Ⅰ.感受、经历、尝试、体验、参与、交流、讨论、合作、参观
Ⅱ.认同、体会、认识、关注、遵守、赞赏、重视、珍惜
Ⅲ.形成、养成、具有、树立、建立、保持、发展、增强
(三)测试的具体内容和要求
化学1
主题1 认识化学科学
主题2 化学实验基础
主题3 常见无机物及其应用
学生实验测试内容①
1.粗盐的提纯
2.蒸馏水的制取
3.用四氯化碳萃取溴水中的溴(或碘水中的碘)
4.配制一定物质的量浓度的溶液
5.常见物质的检验
6.探究金属钠、碳酸钠和碳酸氢钠的性质
7.探究铝及其化合物的性质
8.探究铁及其化合物的性质
9.探究氯气及其化合物的性质
10.探究氨及铵盐的性质
①各模块中学生实验的测试要求参见《化学1》主题2“化学实验基础”。
化学2
主题1 物质结构基础
主题2 化学反应与能量
本文来源:http://www.guakaob.com/jianzhugongchengkaoshi/642422.html
上一篇:八年级上册历史与社会预习
下一篇:淮南师范学院教务系统